DNA Döngüleri Tümörleri Tedaviden Nasıl Kaçırıyor?
Pankreas kanserinin ölümcül esnekliği, tümör hücrelerinin strese hızla adapte olmasını ve tedaviden kaçmasını sağlayan ekstrakromozomal DNA’ya bağlı olabilir.
Pankreas Kanserinde Yeni Bir Oyuncu
Pankreas kanseri en ölümcül kanserler arasındadır ve beş yıllık hayatta kalma oranı sadece %13’tür. Bu korkunç görünüm hem geç teşhis hem de kanserin tedaviye uyum sağlama ve direnme konusundaki olağanüstü yeteneğinden kaynaklanmaktadır. Şimdi, Verona Üniversitesi, Glasgow Üniversitesi ve Botton-Champalimaud Pankreas Kanseri Merkezi’nden araştırmacılar bu uyum yeteneğinin arkasındaki kilit faktörü belirlediler: ekstrakromozomal DNA (ecDNA) – tümörlerin hayatta kalmasına ve gelişmesine yardımcı olabilecek gizli bir genetik sürücü.
Genetik Halkalar: Bir Hayatta Kalma Avantajı
Ekip, bazı pankreas kanseri hücrelerinin, genetik materyalimizin çoğunu barındıran yapılar olan kromozomların dışında bulunan dairesel DNA parçaları üzerinde MYC gibi kritik kanser genlerinin kopyalarını taşıyarak büyük bir hayatta kalma avantajı elde ettiğini buldu. EcDNA olarak bilinen bu genetik halkalar hücre çekirdeğinde serbestçe dolaşarak tümör hücrelerinin gen ifadesini hızla artırmasını, şekillerini değiştirmesini ve başka türlü düşmanca ortamlarda hayatta kalmasını sağlıyor.
Botton-Champalimaud Pankreas Kanseri Merkezi’nde Translasyonel Araştırma Direktörü ve yazar Peter Bailey, “Pankreas kanseri genellikle sessiz bir katil olarak adlandırılır çünkü çok geç olana kadar tespit edilmesi zordur” diyor. “Ölümcüllüğünün bir kısmının tümör hücrelerinin stres altında ‘şekil değiştirme’ yeteneğinden kaynaklandığını biliyoruz. Çalışmamız ecDNA’nın bu hikayenin büyük bir bölümünü oluşturduğunu gösteriyor.”
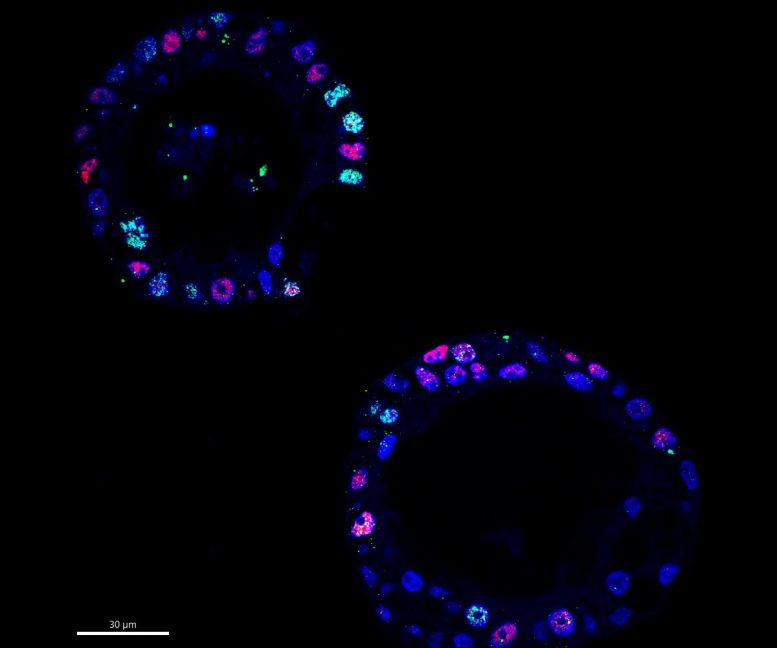
Kanseri teşvik eden MYC proteininin (kırmızı) daha yüksek seviyelerde bulunduğu hücrelerin aynı zamanda yüksek seviyelerde DNA hasarı (yeşil) sergileme eğiliminde olduğunu gösteren immünofloresan görüntüler, çok fazla MYC’nin genomik strese yol açtığını düşündürmektedir. Kredi: Vincenzo Corbo Laboratuvarı.
ecDNA: Kanser Büyümesini Besliyor
Araştırmacılar ecDNA’nın pankreas tümörlerinde, özellikle de kanser büyümesini ve metabolizmasını yönlendiren MYC gibi onkogenler için şaşırtıcı derecede yaygın olduğunu keşfetti. Araştırmanın ilk yazarı ve kıdemli postdoc Elena Fiorini, “MYC ecDNA üzerindeyken MYC kopya sayısında çok daha fazla değişkenlik gördük” diyor. “Bazı hücreler düzinelerce, hatta yüzlerce fazladan MYC kopyası taşıyordu ve bu da onlara belirli koşullar altında büyük bir büyüme avantajı sağlıyordu.”
İlk yazarlardan ve Glasgow Üniversitesi’nin eski doktora öğrencilerinden Daniel Schreyer, “Bu etkili bir ‘bahse girme’ stratejisi” diye ekliyor. “Belirli koşullar altında faydalı olan çok yüksek MYC seviyeleri taşıyan hücre cepleri ve başka bir ortamda daha iyi sonuç verebilecek daha az kopyaya sahip diğerleri elde edersiniz – hepsi aynı tümör içinde.”
Pankreas Tümörlerinin Hedeflenmesindeki Zorluklar
Bu esneklik, sayısız alt popülasyonun bir arada bulunduğu ve tedaviye farklı yanıtlar verdiği pankreas kanserinin karakteristik derin intratümör heterojenliğinin altını çizmektedir. Bir alt kümeyi hedef almak genellikle diğerine karşı başarısız olur ve direnci körükler.
Bu çalışmanın önemli bir avantajı, organoidlerin – laboratuvarda büyütülen pankreas tümörlerinin mini-3D kopyaları – doğrudan erken evre hastalığı olan hastalardan elde edilmiş olmasıdır. Bu organoidler orijinal tümörün genetik yapısının çoğunu koruyor ve bu da onları kanser çalışmaları için mükemmel test ortamları haline getiriyor. Yapay olarak ecDNA ekleyen yöntemlerin aksine, bu laboratuvar modelleri gerçek tümörlerde bulunan gerçek ecDNA varyantlarını yansıtıyor.
Fiorini, “Bu yaklaşım, bir tümörün ne kadar dinamik ve düzensiz olabileceğine dair gerçek dünyadan bilgiler sunuyor” diyor. “İki hastanın her ikisi de ecDNA üzerinde MYC’ye sahip olsa bile, bu dairesel DNA’nın yapısının önemli ölçüde farklılık gösterebileceğini ve bunun da MYC ifadesinde büyük değişikliklere yol açabileceğini ilk elden görüyoruz.”
İş Başında Plastisite: Laboratuvarda Organoidler
Araştırmacılar, ecDNA’nın adaptasyonu nasıl sağladığını görmek için hastadan türetilen organoidleri büyüttüler ve WNT faktörleri gibi hayati büyüme sinyallerini çıkardılar ve ardından bu organoidlerin strese nasıl tepki verdiğini gözlemlediler.
Araştırmanın ilk yazarı ve Verona Üniversitesi’nde eski bir doktora öğrencisi olan Antonia Malinova, “Ekstrakromozomal DNA üzerinde MYC taşıyan organoidlerin WNT’ye olan bağımlılıklarını değiştirebildiklerini gördük” diyor. “Esasen, yüksek düzeyde ecDNA’ya sahip hücreler, hayatta kalmak için artık bu dış sinyallere ihtiyaç duymayarak kendi kendilerine daha yeterli hale geldiler.”
Çalışma ayrıca yüksek MYC seviyeleri ile tümör hücresi şekli ve davranışındaki değişiklikler arasında net bir bağlantı olduğunu ortaya koydu. MYC ecDNA seviyeleri yükseldiğinde, hücreler daha organize, bez benzeri mimarilerini kaybederek daha agresif, katı yapılara dönüştü.
ecDNA: Çift Taraflı Bir Kılıç
“Verona Üniversitesi’nden yardımcı yazar Vincenzo Corbo, “Dikkat çekici olan, bu ecDNA tabanlı kopyaların ortama bağlı olarak ne kadar hızlı ortaya çıkabileceği veya kaybolabileceğidir” diyor. Kanser baskı altındaysa, örneğin temel büyüme faktörlerinden yoksunsa, ecDNA’ya sahip hücreler hayatta kalmak için MYC ifadesini artırabilir. Ancak bu baskı ortadan kalkarsa, çok fazla kopya taşımanın dezavantajlarından kaçınmak için bu ekstra DNA halkalarından bazılarını kaybedebilirler.”
Gerçekten de MYC’nin yüksek seviyelerde ifade edilmesi DNA hasarını tetikleyerek kanser hücrelerini ecDNA tutmanın maliyet ve faydalarını dikkatlice dengelemeye zorlayabilir. “Bu beklenmedik bir durumdu” diyor Corbo. “Daha fazla MYC’nin bir kanser hücresi için her zaman daha iyi olduğu varsayımına meydan okuyor – bu kadar yüksek seviyeleri korumanın gerçek bir uygunluk maliyeti var.”
ecDNA Terapötik Bir Hedef mi?
Ekstrakromozomal DNA bu çalışmada hasta örneklerinin sadece yaklaşık %15’inde görülmesine rağmen, bu alt küme özellikle agresif veya tedavi direncine eğilimli olabilir. Sonuç olarak, ecDNA’yı tespit etmek veya bozmak yeni terapötik pencereler açabilir.
Corbo, “ecDNA tarafından ortaya çıkarılan güvenlik açıklarından yararlanan bir strateji hayal edebiliriz” diyor. “Belki de kanser hücrelerini MYC’yi DNA hasarıyla başa çıkamayacakları bir noktaya kadar çevirmeye zorlamak ya da bu DNA halkalarını koruyan moleküler devreleri bloke ederek hücrelerin bunları tamamen kaybetmesini sağlamak.”
Ancak yazarlar bu tür fikirlerin henüz erken aşamada olduğu konusunda uyarıyor. Corbo, “ecDNA iki ucu keskin bir kılıçtır; hızlı adaptasyon için faydalıdır ancak bakımı maliyetlidir” diyor. “Zor olan, bu dengeyi hasta lehine çevirmektir.”
Kanser Kurallarını Yeniden Yazmak
En önemlisi, bu çalışma genomik plastisite anlayışımızı genişleterek genomun her zaman “sabit” olduğu düşüncesine meydan okuyor. Bailey, “Tümörün çevresinin değişikliklere yol açabileceğini biliyorduk, ancak WNT sinyalinin DNA’yı bu kadar doğrudan yeniden yazabileceğini bilmiyorduk” diye ekliyor. “Çoğunlukla epigenetik değişimler göreceğimizi varsayıyorduk, bu nedenle bu düzeyde bir genomik yeniden mühendislik görmek kesinlikle sürpriz oldu.”
Pankreas kanseri vakalarının önümüzdeki yıllarda artacağı öngörüldüğünde, ecDNA’nın rolüne ilişkin içgörüler, bu genetik özelliği engellemek veya kullanmak için gelecekteki stratejilere rehberlik edebilir – potansiyel olarak tümörleri tedaviye karşı daha savunmasız hale getirebilir.
Kaynak: https://scitechdaily.com
Şiddet Sadece Kişinin Hafızasında Değil, DNA’sında da İz Bırakıyor
