Kanser Gelişiminin Altında Yatan Epigenetik Mekanizmalar Ortaya Çıkarılıyor. Yeni araştırmalara göre kanser gelişimi ve ilerlemesindeki epigenetik mekanizmaların anlaşılmasını geliştirmenin yanı sıra kanser gelişimini yönlendiren genleri saptayarak immünoterapiden fayda görecek hastaların belirlenmesine yardımcı olabilir.
Araştırma, Ürolog Doç. Dr. Qi Cao tarafından yönetilmektedir.
Kansere Bağlı Translasyonel Düzenlemenin İncelenmesi
Northwestern Medicine araştırmacıları, Nature Cell Biology’de yayınlanan bir araştırmaya göre, kanser gelişimini ve ilerlemesini düzenlemede gerekli olan bir proteinin daha önce tanımlanmamış bir rolünü keşfettiler.
Çalışmanın yazarı Cao’ya göre, çalışma ayrıca prostat kanseri ve meme kanserinde bulunanlar gibi solid tümörleri tedavi etmek için potansiyel bir terapötik hedefin altını çiziyor.
Cao “Bu çalışmanın yeniliği, EZH2’nin işlevini translasyonel düzeyinde bulmamızdır. Buna EZH2’nin ‘kanonik olmayan’ işlevi diyoruz.” dedi.
EZH2, solid tümörlerdeki iyi bilinen bir onkojen ve aynı zamanda bir transkripsiyon baskılayıcı olarak tanımlanır — EZH2, protein, DNA üzerindeki belirli bölgelere bağlanarak, çevreleyen genlerin mRNA’ya transkripsiyonunu bloke eder. Ancak Cao’ya göre, EZH2’nin onkogenez ve genel kanser gelişimini düzenlemedeki rolüyle ilgili altta yatan mekanizmaları bilinmemektedir.
Bu çalışmada araştırmacılar, insan prostat kanseri hücre dizilerindeki aktif ribozomları analiz etmek için ribozom profilleme teknolojisini kullandılar. EZH2’nin kanser hücrelerinde iki önemli RNA modifikasyonunu ve translasyon sürecini düzenlediğini keşfettiler: Bir çeşit metilasyonu bozmak ve ribozomda belirli bir translasyon başlangıcını azaltmak.
Yazarlara göre, bulgular, EZH2 yüksek kanser hücrelerinde transkripsiyon ve translasyonu düzenlemede EZH2’nin ikili rolünü, ribozom fonksiyonlarını hızlandırarak ve kanserle ilgili translasyon kontrolüne katkıda bulunarak kanserin ilerlemesine teşvik ettiğini gösteriyor.
Ayrıca, EZH2’yi metiltransferaz olmayan rollerinden arındırarak ele almak, solid tümörleri tedavi etmek için etkili bir terapötik yaklaşım olabilir. Yazarlara göre, mevcut EZH2 ele alma stratejileri ağırlıklı olmak üzere EZH2’nin lizin metiltransferaz aktivitesini inhibe etmeye odaklandığından -ki önceki çalışma solid tümör ilerlemesini tamamen inhibe edemediğini ortaya çıkarmıştır- bu yeni yaklaşım teşvik edici olacaktır.
Yazarlar, “Sonuçlarımız, EZH2’nin onkogenezde lizin olmayan metiltransferaz rolünün önemini ortaya çıkardı. Bu sonuçlar, metiltransferaz olmayan rollerinin ortadan kaldırılmasında uzmanlaşmış EZH2 ele alma stratejilerinin geliştirilmesi için özgün perspektifler sağlayabilir.” diye yazdı.
Molecular Cell dergisinde yayınlanan bulgulara göre metiltransferaz olmayan rollerinin ortadan kaldırılmasında uzmanlaşmış EZH2 ele alma stratejilerinin geliştirilmesi için diğerlerinden farklı bakış açıları sağlayabilen exitron splicing (EIS) ile zenginleştirilmiş genler, kanser gelişimi sürecini hızlandırabilir ve ümit verici terapötik bir hedef görevini görebilir. Cao Laboratuvarı’nda doktora sonrası araştırmacı olan Dr. Cao ve Qi Liu, çalışmanın ortak yazarıydı.
Uçbirleştirme (splicing), yeni yapılan mRNA’nın olgun mRNA’ya dönüştürüldüğü bir süreçtir. Bu işlem sırasında, intronlar (RNA’nın protein kodlamayan bölgeleri) çıkarılır ve eksonlar (RNA’nın protein kodlayan bölgeleri) bir araya getirilir.
Alternatif bir uçbirleştirme çeşidi, bazı intronların genellikle bir RNA sekansından kesilerek korunduğu EIS’dir; bu, protein yapısı ve işlevini değiştiren ve genetik değişikliklerin sonucunu taklit edebilen bir RNA dizisi olan exitron adı verilen bir “kriptik intron” yaratır.
Exitronlar spesifik olarak eksonların eklenmiş iç bölgeleridir ve normal koşullar altında tutulur. Eksonların iç kısımları oldukları için, normalde bir mRNA dizisinin translasyon sürecinin sonunu işaret eden durdurma kodonları içermezler.
Yazarlara göre, EIS tam olarak anlaşılmamış olsa da, son araştırmalar kanserde EIS’nin bir rolü olduğunu, özellikle de exitron-spliced mRNA’lar tarafından kodlanan proteinlerin kanser gelişimine katkıda bulunabileceğini öne sürüyor.
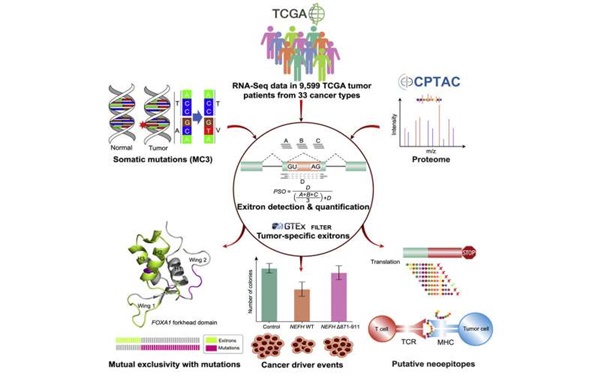
Bu çalışma için araştırmacılar, 33 kanser türünde 10.000 numuneden alınan transkriptom sekansı verisini analiz ettiler ve EIS’nin insan kodlama genlerinin yüzde 63’ünü etkilediğini keşfettiler ki bunların %95’i tümör spesifikti.
Cao, “Bu, genlerin yalnızca yüzde 4’ünün EIS gösterdiğini belirten önceki çalışmaları önemli seviyede detaylandırıyor.” dedi.
Ayrıca, significantly exitron-spliced genler (SEG’ler) için zenginleştirilmiş genlerin, kanserde significantly mutated genlerle karşılıklı olarak dışlandıklarını buldular. SEG’lerin daha ileri analizi, prostat kanserinde yeni bir tümör baskılayıcı olarak NEFH genini ortaya çıkardı.
Önceki çalışmalar, tümör hücrelerinde oluşan ve vücudun kansere karşı bağışıklık tepkisinde rol oynayan proteinler olan tümör neoantijenlerinin üretilmesinde mRNA uçbirleştirmesinin rolünü de göstermiştir. Cao’ya göre bu çalışma, mevcut bulgularla birleştiğinde, immünoterapiye en iyi yanıt veren hastaların belirlenmesine ve yeni tedavi stratejilerinin geliştirilmesine yardımcı olabilir.
Cao “Bulgularımız, EIS’nin genetik değişikliklerin ötesinde ek bir kansere neden olan mekanizmayı temsil ettiğini belirtmektedir. Ayrıca, analizlerimiz EIS kaynaklı neoantijen yükünün kanser immünoterapi yanıtı için aday bir prediktör olduğunu ortaya koymaktadır.” dedi.
Bulgular, SEG’lerin kanser tetikleyici genler olma potansiyeline sahip olduğunu ortaya koyarken çoğu SEG üzerine yeterince araştırma yapılmamıştır. Cao, sonraki adımlar için ekibin SEG’lerin işlevlerini sistematik olarak karakterize etmeyi umduğunu söyledi.
Cao “Ek olarak, EIS’den türetilen neoantijenlerin immünojenisitesine ilişkin mevcut analizimiz, esas olarak halihazırda mevcut olan herkese açık veri kümelerine dayanıyordu. Tümör veya periferik kandaki tanımlanmış neoantijenlerin T hücresini tanımasını deneysel olarak göstermek için yapılacak daha fazla çalışma, klinik deneylerde kanser immünoterapi hedeflerine öncelik vermek için kritik olacaktır” dedi.
Kaynak: https://phys.org/
Kanser Gelişiminin Altında Yatan Epigenetik Mekanizmalar Ortaya Çıkarılıyor
Çeviri: Ece Nur Öngören
Kanser Gelişiminin Altında Yatan Epigenetik Mekanizmalar Ortaya Çıkarılıyor