CRISPR’ın Derinliklerinde Yeni Bir Kalkan Keşfedildi
Dünya üzerinde yaşayan her canlının kendisine zarar verebilecek şeylerden kendini koruması gerekir. Bakteriler de farklı değildir. Ve göreceli basitliklerine rağmen, viral istilacılara karşı oldukça akıllıca savunma stratejileri uygularlar. Bunlardan en bilineni, FDA onaylı ilk genetik düzenleme tekniği olarak insan kullanımına uyarlanan CRISPR-Cas9‘dur.
Geçtiğimiz yıl, Luciano Marraffini başkanlığındaki Rockefeller Bakteriyoloji Laboratuvarı ve Dinshaw Patel başkanlığındaki MSKCC Yapısal Biyoloji Laboratuvarı araştırmacıları, CARF efektörleri olarak adlandırılan bazı CRISPR sistemlerinin temel bağışıklık bileşenlerini incelediler. Yeni keşfedilen bu silahlar aynı hedefe ulaşmak için farklı yaklaşımlar benimsiyor: bir virüsün bakteri popülasyonunun geri kalanına yayılmasını önleyen hücresel aktiviteyi durdurmak.
Science dergisinde yakın zamanda yayımlanan bir makalede araştırmacılar, keşfettikleri ve Cat1 adını verdikleri en yeni CARF efektörünü duyurdular. Alışılmadık derecede karmaşık moleküler yapısı sayesinde bu protein, hücresel işlev için gerekli olan bir metaboliti tüketebilir. Yakıtsız kalan viral istilacının daha ileri bir saldırıya geçme planları durma noktasına geliyor.
Marraffini, “Laboratuvarlarımızın kolektif çalışması, bu CARF efektörlerinin ne kadar etkili ve farklı olduğunu ortaya koyuyor” diyor. “Moleküler aktivitelerinin çeşitliliği oldukça şaşırtıcı.”
Çoklu savunma sistemleri
CRISPR, bakterilerin ve diğer bazı tek hücreli organizmaların adaptif bağışıklık sistemlerinde bulunan ve faj adı verilen virüslere karşı koruma sağlayan bir mekanizmadır. Altı tip CRISPR sistemi kabaca aynı şekilde çalışır: Bir CRISPR RNA yabancı genetik kodu tanımlar, bu da bir bağışıklık tepkisine aracılık etmesi için bir cas enzimini tetikler ve genellikle istilacı materyali keser.
Ancak giderek artan sayıda kanıt, CRISPR sistemlerinin genetik makasın ötesinde çok çeşitli savunma stratejileri uyguladığını gösteriyor. Marraffini’nin laboratuvarı bu araştırmanın çoğuna öncülük etmiştir. Özellikle, CRISPR-Cas10 sistemlerinde CARF efektörleri olarak adlandırılan ve bir bakterinin faj enfeksiyonu üzerine aktive olan proteinler olan bir molekül sınıfını inceliyorlar.
CARF efektör bağışıklığının, viral replikasyon için misafirperver olmayan bir ortam yaratarak çalıştığına inanılmaktadır. Örneğin, Cam1 CARF efektörü enfekte olmuş bir hücrenin membran depolarizasyonuna neden olurken, Cad1 enfekte olmuş bir hücreyi toksik moleküllerle doldurarak bir tür moleküler fumigasyonu tetikler.
Metabolik dondurma
Mevcut çalışma için, araştırmacılar ek CARF efektörlerini tanımlamaya çalışmak istediler. Cat1’i bulmak için güçlü bir yapısal homoloji arama aracı olan Foldseek’i kullandılar.
Cat1’in, siklik tetra-adenilat veya cA4 adı verilen ikincil haberci moleküllerin bağlanmasıyla bir virüsün varlığına karşı uyarıldığını ve bunun da enzimi hücrede NAD+ adı verilen temel bir metaboliti parçalaması için uyardığını buldular.
Marraffini laboratuvarında TPCB yüksek lisans öğrencisi olan ilk yazar Christian Baca, “Yeterli miktarda NAD+ parçalandığında, hücre bir büyüme duraklama durumuna girer” diyor. “Hücresel işlev durakladığında, faj artık çoğalamaz ve bakteri popülasyonunun geri kalanına yayılamaz. Bu şekilde Cat1, Cam1 ve Cad1’e benziyor, çünkü hepsi de popülasyon düzeyinde bakteriyel bağışıklık sağlıyor.”
Eşsiz karmaşıklık
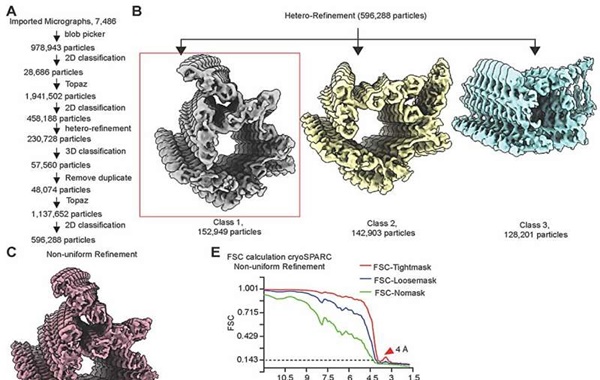
Ancak bağışıklık stratejisi bu diğer CARF efektörlerine benzese de, Patel Laboratuvarı’nda doktora sonrası araştırma bursiyeri olan ilk yazar Puja Majumder’in kriyo-EM kullanarak yaptığı ayrıntılı yapısal analizle ortaya koyduğu gibi, şekli öyle değil.
Cat1 proteininin, Cat1 dimerlerinin cA4 sinyal molekülü tarafından yapıştırıldığı, viral enfeksiyon üzerine uzun filamentler oluşturduğu ve NAD+ metabolitlerini yapışkan moleküler cepler içinde hapsettiği şaşırtıcı derecede karmaşık bir yapıya sahip olduğunu buldu. Majumder, “NAD+ metaboliti Cat1 filamentleri tarafından parçalandıktan sonra, hücrenin kullanması için mevcut değildir” diye açıklıyor.
Ancak proteinin tekil yapısal karmaşıklığı burada bitmiyor, diye ekliyor. “Filamentler trigonal spiral demetler oluşturmak için birbirleriyle etkileşime giriyor ve bu demetler daha sonra beşgen spiral demetler oluşturmak için genişleyebiliyor” diyor. Bu yapısal bileşenlerin amacı araştırılmaya devam ediyor.
Cat1’in genellikle tek başına çalışıyor gibi görünmesi de alışılmadık bir durum. Baca, “Normalde tip III CRISPR sistemlerinde, bağışıklık etkisine katkıda bulunan iki faaliyetiniz vardır” diyor. “Ancak, Cat1’i kodlayan bakterilerin çoğu bağışıklık etkisi için öncelikle Cat1’e güveniyor gibi görünüyor.”
Marraffini, bu bulguların ilgi çekici yeni sorular ortaya çıkardığını söylüyor. “Büyük resmi – CARF efektörlerinin faj replikasyonunu önlemede harika olduğunu – kanıtladığımızı düşünürken, bunu nasıl yaptıklarının ayrıntıları hakkında hala öğrenecek çok şeyimiz var. Bu çalışmanın bizi bundan sonra nereye götüreceğini görmek büyüleyici olacak.”
Kaynak: https://phys.org/news
CRISPR Teknolojisi Bağışıklık Sisteminin Kanseri Yok Etmesini Kolaylaştırdı